成人の急性呼吸器感染症の治療:多施設無作為化二重盲検プラセボ対照臨床試験の結果。 臨床試験における無作為化 無作為化対照二重盲検試験
抗がん剤はさまざまで、それぞれが特定の目的のために実施され、医薬品研究に必要なパラメーターに従って選択されます。 現在、次のタイプが区別されています 臨床研究:
オープンおよびブラインドの臨床試験
臨床試験はオープンまたはブラインドの場合があります。 研究を開く- これは、医師と患者の両方がどの薬が調査されているかを知っているときです. 盲検シングルブラインド、ダブルブラインド、フルブラインドに分けられます。
- 簡易盲検一方の当事者がどの薬物が調査されているかを知らない場合です。
- 二重盲検試験と 全盲検 2 つ以上の当事者が治験薬に関する情報を持っていない場合です。
パイロット臨床試験研究のさらなる段階を計画するために重要な予備データを取得するために実行されます。 簡単に言えば、それを「目撃」と呼ぶことができます。 パイロット研究の助けを借りて、より多くの被験者について研究を実施する可能性が決定され、将来の研究に必要な能力と経済的費用が計算されます。
対照臨床試験- これは、有効性と安全性がまだ十分に研究されていない新しい (治験) 薬と、標準的な治療法、つまり、すでに研究に合格して市場に参入した薬と比較する比較研究です。
最初のグループの患者は治験薬による治療を受け、2番目の患者は標準(このグループは呼ばれます コントロール、したがって研究の種類の名前)。 コンパレータは、標準療法またはプラセボのいずれかです。
非管理臨床試験- これは、対照薬を服用している被験者のグループが存在しない研究です。 通常、この種の臨床試験は、有効性と安全性が証明されている医薬品に対して実施されます。
無作為化臨床試験患者を複数のグループ(治療の種類または投薬レジメンによって)に無作為に割り当て、治験薬または対照薬(対照薬またはプラセボ)を投与する機会を同じにする研究です。 の 無作為化されていない研究無作為化手順はそれぞれ実行されず、患者は別々のグループに分けられません。
並行およびクロスオーバー臨床試験
並行臨床試験- これらは、異なるグループの被験者が治験薬のみまたは対照薬のみを受ける試験です。 並行研究では、被験者のいくつかのグループが比較され、そのうちの1つは治験薬を受け取り、もう1つのグループは対照です。 いくつかの並行研究では、対照群を含めずに異なる治療法を比較しています。
クロスオーバー臨床試験各患者がランダムな順序で両方の薬を比較する研究です。
前向きおよび後ろ向きの臨床試験
前向き臨床研究- これは、転帰 (研究者の関心の対象となる臨床的に重要な事象 - 寛解、治療への反応、再発、死亡) が発生するまで、患者グループを長期間にわたって観察することです。 このような研究は最も信頼できるため、最も頻繁に実施され、同時にさまざまな国で、つまり国際的です。
前向き研究とは異なり、 後ろ向き臨床研究それどころか、以前の臨床試験の結果が研究されています。 結果は、研究が始まる前に発生します。
単一および多施設臨床試験
臨床試験が単一の研究センターで行われる場合、それは呼ばれます シングルセンター、および複数に基づく場合、 多施設. ただし、研究が複数の国で実施される場合(原則として、センターは異なる国にあります)、それは呼ばれます 国際的.
コホート臨床研究参加者の選択されたグループ(コホート)をしばらく観察する研究です。 この期間の終わりに、研究の結果は、このコホートの異なるサブグループの被験者間で比較されます。 これらの結果に基づいて、結論が導き出されます。
前向きコホート臨床研究では、被験者のグループが現在形成され、将来観察されます。 レトロスペクティブ コホート臨床研究では、アーカイブ データに基づいて被験者のグループが選択され、その結果が現在まで追跡されます。

どのタイプの臨床試験が最も信頼できるでしょうか?
の 近々、製薬会社は臨床試験を実施する義務があります。 最も信頼できるデータ. ほとんどの場合、これらの要件を満たしています 前向き、二重盲検、ランダム化、多施設共同、プラセボ対照研究. だということだ:
- 見込みのある– 長期間監視されます。
- ランダム化-患者はランダムにグループに割り当てられました(通常、これは特別なコンピュータープログラムによって行われるため、最終的にグループ間の違いは重要ではなくなり、統計的に信頼できなくなります)。
- ダブルブラインド- 医師も患者も、無作為化中に患者がどのグループに分類されたかを知らないため、そのような研究は可能な限り客観的です。
- マルチセンター-一度に複数の機関で実施されます。 一部の種類の腫瘍は非常にまれであり (たとえば、非小細胞肺がんにおける ALK 変異の存在)、プロトコルの選択基準を満たす必要な数の患者を 1 つのセンターで見つけることは困難です。 したがって、そのような臨床研究は、いくつかの研究センターで一度に実施され、原則として、同時にいくつかの国で実施され、国際的と呼ばれます。
- プラセボ対照– 参加者は 2 つのグループに分けられます。一方は治験薬を受け取り、もう一方はプラセボを受け取ります。
ランダム化比較臨床試験(RCT)、 治療、診断、および疾患のための手段、方法、レジメンの潜在的な有効性を評価するために、病院で実施されますが、他の医療施設で実施されることはあまりありません。
病気の治療のために提案された薬の潜在的な有効性を評価する場合、集団は、この病気の同じ臨床経過、比較的同じ性別と年齢、および病気の転帰に影響を与える可能性のある他の徴候を持つ患者です。
サンプルは特定の制限を考慮して形成されますが、患者は母集団を代表し、 サンプルには含まれていません 主に次の理由によります。
実験的治療の期待される効果に影響を与える可能性のある要因の選択基準の不遵守;
実験への参加の拒否;
個人が実験の条件を遵守していない可能性があると認識されていること(たとえば、処方薬の不規則な摂取、交渉可能性の規則の違反など);
実験的治療の禁忌。
このような選択の結果、形成されたサンプルが小さいことが判明する可能性があり、実験群と対照群の結果の頻度の違いの信頼性を評価する結果に影響を与えます。 また、成形されたサンプルはシャープにできます。 移動した また、信頼できるデータであっても、結果を患者集団全体に拡張すると、重大な制限が生じます。
ランダム化 RCT では、以下に従ってグループの比較可能性を確保する必要があります。 さまざまな兆候最も重要な、 病気の転帰に影響を与える徴候 . ただし、これは常に形成できるとは限らない、十分に大きなサンプルでのみ達成できます。 少数の患者では、グループの比較可能性は、原則として、さまざまな理由で一部の人々が実験から脱落し、信頼できる結論を妨げる可能性があるという事実の結果として違反されます。
米。 7. 心筋梗塞患者の早期退院の結果を評価するためのランダム化比較試験. ソース. 疫学の基礎。 Rビーグルホール等。 WHO、ジュネーブ、1994 年。
与えられたデータ (図 7) は、さまざまな理由で、実験に参加する患者の数がどのように急激に減少したかを示しています。 その結果、統計処理の結果は信頼できないことが判明し、この研究のデータによると、心筋梗塞を起こした人にとって早期退院(3日後)は安全であると非常に暫定的に仮定することしかできません.
信頼性を下げるには RCT で使用されるランダム化方法は、ほとんどの場合、次の順序で配布されます。
独立した統計学者、または製薬会社の代表者による電話による集中無作為化。
製薬会社が提供するコード化(番号付け)された同一の容器の方法。容器のコードと内容は、研究に参加している患者または医師のいずれにも知られていない。
集中型コンピューター法 - コンピューター プログラムは、乱数表のシーケンスと同様に、患者をグループにランダムに分布するシーケンスを生成します。 同時に、患者の比較グループへの分割は、無作為化プロセスにのみ参加する専門家によって行われます。
不透明で密封され、番号が付けられた封筒の方法。 必要な介入に関する指示は、乱数の表に従って順番に番号が付けられた封筒に入れられます。 入院部門の研究者が患者の名前やその他の必要なデータを書き留めてから封筒を開封することが非常に重要です。
方法に関係なく、無作為化は可能です。 シンプルで階層化された (他にも、あまり一般的ではないタイプのランダム化があります)。 単純な無作為化の場合、追加の要因は考慮されず、各患者は 50/50 の確率でいずれかのグループに分類されます。 層別無作為化(サブグループの選択 - 階層)は、被験者の経験の結果を同じ予測でグループを作成することが不可能な場合に使用されます。 たとえば、与えられたパラメーター (年齢、血圧レベル、心筋梗塞など) の 1 つが研究の結果に影響を与える可能性がある場合、患者は最初にサブグループに分けられます。 さらに、各サブグループでは、グループがランダム化されます。 一部の専門家は、層化無作為化が不十分であると考えています。
研究結果の信頼性を読者が評価するための無作為化方法に関する情報の重要性にもかかわらず、さまざまな著者がこのパラメーターに関する研究についてほぼ同じ評価を行っています。 1980 年代と 1990 年代に、専門誌に掲載された RCT レポートの 25 ~ 35%、一般的な医学雑誌に掲載されたレポートの 40 ~ 50% のみが、参加者をグループにランダムに含める順序を生成する正しい方法を使用して報告されたことがわかりました。 . これらのケースのほとんどすべてで、コンピュータージェネレーターまたは乱数テーブルが使用されました。 22 年間に皮膚科学の雑誌の 1 つに掲載された記事の分析では、ランダムな配列を生成するための正しい方法の使用が 68 の RCT レポートのうち 1 つだけで報告されていることがわかりました。
治療の RCT を編成する上で最も重要な要素は、盲検化 (マスキング) 法の使用です。 前のセクションで示したように、試験に参加している患者または医療関係者は、無意識または意図的にデータを歪め、それによって試験の結果に影響を与える可能性があるため、二重盲検および三重盲検試験が好まれます。
適用された介入の結果は、患者の心理状態に大きく依存するため、患者からの介入をマスキングすることは重要です。 情報が公開されていると、実験グループの患者は、治療の好ましい結果を不当に期待するか、逆に、「モルモット」になることに同意したという事実を心配する可能性があります. 対照群の患者は、特に治療プロセスが実験群でより成功していると信じている場合、取り残されていると感じるなど、異なる行動をとる可能性があります. 患者のさまざまな心理状態は、健康状態の改善またはその逆の兆候の意図的な検索につながる可能性があり、それは必然的に自分の状態の評価に影響を与え、その変化はしばしば想像上のものになります. 医師研究者からのマスキングが必要です。なぜなら、彼はテストされた薬の利点を明らかに確信し、被験者の健康状態の変化を主観的に解釈できるからです。
二重マスキングの必要性は、「プラセボ効果」を客観的に確認します。 プラセボ - 剤形、外観、色、味、匂いにおいて治験薬と見分けがつかないが、特定の効果はありません。または、プラセボ効果に関連するバイアスを排除するために治療をシミュレートするために医学研究で使用されるその他の無関心な介入. プラセボ効果 - 薬物の生物学的効果ではなく、治療の事実のみに関連する患者の状態の変化(患者自身または主治医によって指摘される)。
多数の研究により、一部の患者 (疾患によって最大 3 分の 1 まで) が薬の代わりにプラセボを服用し、実験群の患者と同じように、またはほとんど同じように反応することがわかっています。 プラセボ効果を研究すると明らかになる 明確 新しい治療の成分。 さらに、患者が自分がどのグループに属しているのかわからない場合、実験のルールにより正確に従います。
前のセクションで述べたように、結論の信頼性を向上させるために、次のことを導入します。 三度目の失明 統計データ処理の段階で、これらの行為を独立した人物に委託する。
ブラインド臨床試験は使用されていません 外科的介入、理学療法、食事療法、多くの診断手順などの潜在的な有効性を評価するとき、すなわち 効果を隠すことが不可能な場合、または患者または医師にとって不適切な場合。 そのような場合、無作為化試験が呼び出されます 開ける。
設定された観察時間の後、実験群と対照群で特定された疾患の結果(効果)の統計処理が実行されます。 系統的エラーを回避するために、患者の実験群と対照群における疾患の転帰の基準は具体的で同じでなければなりません。 結論の信頼性を高めるために、研究は一度にではなく、新たに到着した患者を含めて一定期間にわたって実施されることがよくあります。
得られたデータの統計処理には、同じ2×2テーブルを使用します。

表 11. 実験的研究の結果を評価するための 2 x 2 テーブルのレイアウト。
臨床試験および野外試験における実験的曝露の有効性を評価する指標のほとんどは、(歴史的に)他の名前を持っていますが、計算方法と意味の両方で、コホート研究で計算された値に対応しています。
効果を定量化するために、さまざまな統計指標が使用されますが、それらの名前の厳密な統一はありません。
1.
相対効率指標 (
業績指標
):

この値は、コホート研究で計算された相対リスクに対応します。 . パフォーマンス インジケータによって決定されます。 何回 、実験群における曝露の肯定的な結果の頻度は、対照群におけるそれらの頻度よりも高い、すなわち 何回 一般的に使用されている方法よりも優れた新しい治療法、診断法など。
評価基準は、業績指標を解釈するために使用されます 相対危険度 (コホート研究の統計処理を参照)。 同時に、評価されるのは疾患の危険因子ではなく、適用された実験的影響の有効性であるため、表現の意味はそれに応じて変化します。
2. 属性(追加)効果 、コホート研究で決定された属性 (追加) リスクに対応します。

属性効果の大きさが示す いくら 実験的曝露の影響は、対照群における曝露の影響よりも大きい。
3 . 影響の影響の割合(効率の割合) コホート研究からのデータの分析で計算された病因の割合に対応します。

この値は、実験グループの肯定的な効果の合計における、実験的曝露に起因する肯定的な結果の割合を示しています。
4. と呼ばれる追加の値 - 1 つの有害な結果を防ぐために治療する必要がある患者の数 (NNT)。

この指標が高いほど、調査された影響の潜在的な有効性が低くなります。
コホート研究のデータ処理と同様に、実験で得られたデータの信頼性はカイ二乗検定などの方法で評価されます。
結論として、すべての利点にもかかわらず、無作為臨床試験は偏り、特にサンプリングエラーの可能性をはらんでいます。 したがって、ある研究の結果は、たとえその組織が完璧であっても、臨床現場での新薬の使用に対する無条件の推奨と見なすことはできません. そのため、現時点では結果のみが信頼できると考えられています。 多施設研究 いくつかの診療所による同じ介入(治療)の有効性。ただし、異なる国の診療所で研究を実施することが望ましい。
ランダム化臨床試験にはどのような種類がありますか? ランダム化臨床試験の利点と欠点
無作為化試験は、オープンまたはブラインド (マスク) にすることができます。 無作為化試験は、無作為化の直後に患者と医師の両方がこの患者にどのような種類の治療が使用されるかを知った場合、未解決であると見なされます。 実践的なクラスでは、学生は「ブラインド」スタディのデザインを簡単かつ迅速に記憶できます。 盲検研究では、患者は使用された治療の種類について知らされておらず、この瞬間は、受領時に事前に患者と話し合っています。 インフォームドコンセント研究のために。 医師は、無作為化手順の後に患者が受ける治療オプションを知ることができます。 二重盲検研究では、医師も患者も、特定の患者にどの介入が使用されているかを知りません。 三重盲検試験では、介入の種類は、患者、医師、および試験結果を処理する研究者 (統計学者) にはわかりません。 現在、世界の慣行では、二重または三重盲検対照によるランダム化比較(前向き)試験が「ゴールドスタンダード」と見なされています。
研究は、単一施設または多施設で行うことができます。 多施設RCTを実施する場合、いくつかの機関が試験に参加するため、短時間ですべての予後徴候に関して均質な大規模なサンプルが確実に形成されます。
ランダム化比較試験のメリットとデメリット
利点:
- · 研究の結果は研究者の意見に左右されず、系統誤差は大きな影響を与えません。 グループ間に違いがないことを保証します。
- 最も説得力のある実行方法
- 既知および未知の交絡因子の制御
- その後のメタ分析の可能性
欠陥:
- ・ 高価。
- · 方法論は複雑であり、患者選択の複雑さ (通常、研究がどれほど大規模であっても、この疾患の患者全体の 4 ~ 8% しか含めることができません)。母集団への結果、つまり この研究で証明された結果は、無作為化試験に含まれる患者と同一の患者にのみ拡張できます。
- · 倫理的な問題。
ある部門の6年目に、教師は私たちのグループに質問をしました。 特定の疾患の治療薬はどのような根拠に基づいて推奨されますか?"。 一部の学生は、作用機序や疾患の特徴などに基づいて薬を選択することを提案しました。 これらは完全に正確な答えではありません。 今日、薬は主に彼らのために選ばれます 効率. そして、彼らはそれを行います 厳密な科学的方法. 今日は次のことを学びます。
- 縦方向または横方向のどちらの研究が安価であるか、
- おしゃぶりは子供だけのものではなく、
- ブラインド治療が最も価値があると考えられている理由。
現代の治療法は体位に基づいています 根拠に基づいた医療 (根拠に基づいた医療). « 根拠に基づいた医療"、"とも呼ばれます。 臨床疫学"。 エビデンスに基づく医療は、数学的統計学の厳密な科学的方法を使用して研究された多くの同様のケースの経過に基づいて、特定の患者の病気の経過を予測することを可能にします。
薬の有効性または非効率性について結論を出すには、調査を行います。 前 医薬品彼は実際の患者によってテストされ、生きた組織、動物、健康なボランティアで多くの実験を受けます. これらの段階については、資料「医薬品の開発方法」で個別に詳しく説明します。 最後に、薬の有効性と安全性が病気の人々のグループでテストされ、そのようなテストは呼ばれます 臨床.
臨床研究を準備する際、科学者は被験者の条件、選択および除外基準、研究中の現象を分析するための方法論などを決定します。 これらすべてをまとめて呼びます 研究デザイン.
臨床試験の種類
存在する 3種類の臨床試験独自の長所と短所があります。
- 横断的(同時)研究、
- 縦断的(前向き、縦断的、コホート)研究、
- 回顧的研究(「ケース - コントロール」)。
次に、各タイプについて詳しく説明します。
1) 横断的(一発)研究.
これ 患者グループの単一検査. たとえば、研究グループにおける疾患の発生率と現在の経過に関する統計を取得できます。 特定の時点で撮影された写真を思い出します。 横断研究は安価ですが、そこから病気のダイナミクスを理解することは不可能です。
例:企業のショップドクターの予防検査。
2) 縦断(前向き、縦断、コホート)研究.
用語: 緯度から。 縦筋- 縦。
縦断研究は、 患者グループの長時間の観察. 今日まで、そのような研究はそれ自体が信頼できる (証拠に基づく) ため、最も頻繁に実施されています。 ただし、それらは高価であり、ほとんどの場合、同時に複数の国で実行されます (つまり、国際的です)。
縦断研究がコホート研究とも呼ばれるのはなぜですか? コホート -
- 古代ローマの軍団の戦術単位 (紀元前 2 世紀以降)。 軍団には10のコホートがあり、コホートには360〜600人がいました。
- 比喩的な意味で、緊密に結ばれた人々のグループ。
- 臨床疫学では コホート- もともと何人かによって団結した人々のグループです 共通機能(例: 健康な個人または病気の特定の段階にある患者) および特定の期間にわたって観察されます。
1グループにおける研究モデルのスキーム.
前向き研究の中には、単純および二重盲検、オープンなどがあります。これについては、以下で詳しく説明します。
3) レトロスペクティブ研究 (「ケース - コントロール」).
これらの研究は、過去の危険因子と患者の現在の状態を関連付ける必要がある場合に実施されます。 最も単純な例: 患者が心筋梗塞を起こし、地域の医師がカードをめくって次のように考えました。 確かに、数年間の高コレステロールはうまく終わらない. 患者はより多くのスタチンを処方されるべきです».
後ろ向き研究は安価ですが、エビデンスは低いです。 過去の情報は信頼できません (たとえば、外来カードはさかのぼって、または患者を検査せずに記入される可能性があります)。
二重盲検無作為多施設プラセボ対照試験
上で述べたように 最も証拠それは 前向き(縦断的)研究、これが最も頻繁に実行される理由です。 これまでのすべての前向き研究の中で最も信頼できるものは、 二重盲検無作為多施設プラセボ対照試験. 名前は科学的すぎるように見えますが、複雑なことは何もありません。 単語ごとに説明しましょう。
何が起こったか 無作為化試験? その言葉は英語から来ています。 ランダム化- ランダムな順序で並べます。 ミックス。 テストされた薬の有効性は何かと比較する必要があるため、すべての研究には 経験者グループ(必要な薬がチェックされています)および 対照群、 また 比較群(対照群の患者には試験薬を投与しない)。 先を見据えて、対照群を用いた研究が呼び出されると言います 制御された.
この場合のランダム化は、グループへの患者のランダムな分布です。 研究者が自分の利己的な目的のために、実験群で軽度の患者を収集し、対照群でより重症の患者を収集できなかったことは非常に重要です. 無作為化には特別な方法があるため、最終的にグループ間の違いは統計的に信頼できなくなります。 コンセプトについて 信憑性» エビデンスに基づく医療では、さらに詳しく説明します。
何が起こったか 盲検と二重盲検? で 孤独なブラインドこの研究では、患者は無作為化中に自分がどのグループに分類され、どの薬が投与されたかを知りませんが、医療従事者はこれを知っています。 で ダブルブラインド研究では、医師も患者も、特定の患者が何を受け取っているかを正確に認識していないため、そのような研究はより客観的です.
ノート。 なんらかの理由でプラセボを使用できない場合 (たとえば、医師または患者がその効果によってその薬を容易に認識できる。たとえば、MgSO4 を静脈内投与すると、内側から激しい熱の短い感覚が生じる)、 研究を開く(医師と患者の両方が、どの薬が処方されているかを知っています)。 ただし、公開研究は信頼性がはるかに低くなります。
興味深いことに、病院の患者の総数のうち プラセボ(ダミードラッグ; プラセボはドラッグを模倣しますが、 活性物質含まれていません)が役立ちます 25-35% 、精神疾患の場合 - 最大40%。 プラセボを投与された患者が顕著な効果を示した場合、そのような患者は研究から除外される場合があります。
プラセボの代わりに、テストと比較したい薬を使用できます。 次に、テストされた薬は2つのオプションのいずれかで服用できます。
- 並行グループで: すなわち 1 つのグループでは治験薬を服用し、2 つ目の(対照)グループではプラセボまたは対照薬を服用します。
パラレルグループ学習モデルの概要.
- クロススタディで: 特定の順序で各患者に試験薬と対照薬を投与します。 前の薬を服用したことによる影響を「排除」するように設計された、これらの薬の服用の間には自由な期間が必要です. そのような期間は呼ばれます 清算"、 また " 洗濯».
「クロス」研究モデルのスキーム.
何が起こったか 制御された研究? 先ほど述べたように、これは 2 つの患者グループを対象とした研究です。 経験者グループ(新薬または新治療を受ける)および 対照群(受け取っていません)。 ただし、小さな問題があります。 対照群の患者に薬が投与されない場合、彼らは治療を受けていないと判断し、気分を害して落ち込んでしまいます. 治療の結果は間違いなく悪化します。 そこで、研究者は対照群にプラセボ、つまりダミーを与えます。
エビデンスに基づく医療における管理の種類:
- に 外観プラセボの味は、活性物質を含まない特別な賦形剤のおかげで、試験中の薬物に似ています. このタイプのコントロールは、 プラセボ コントロール (ネガティブ コントロール).
- プラセボを服用している患者が治療の欠如によって重大な害を受ける可能性がある場合、プラセボは 有効な薬比較。 このタイプのコントロールは、 アクティブ(ポジティブ). アクティブコントロールは、プロモーション目的でも使用され、 新薬既存のものを凌駕します。
- 履歴管理、 また アーカイブ統計管理. 次の場合に使用 効果的な方法病気の治療法はなく、比較するものは何もありません。 この場合、治療の結果は、そのような患者の通常の生存率と比較されます。
例: ある種の癌治療、移植術の開発の初期段階における臓器移植手術。
- 初期状態制御. 患者を検査し、治療結果を実験的治療前の初期状態と比較します。
完全を期すために、さらに 2 つのまれな制御方法についても言及します。
多施設いくつかの「センター」、つまり診療所ですぐに行われる研究と呼ばれます。 一部の疾患は非常にまれであり (たとえば、特定の種類の癌)、1 つのセンターの特定の時点で、研究の選択基準を満たす適切な数のボランティア患者を見つけることは困難です。 通常、このような研究は費用がかかり、国際的な複数の国で実施されます。 たとえば、ミンスクの多くの病院も参加しました。
制御期間
すべての研究は コントロール(導入)期間その間、患者は命を救うもの(狭心症のニトログリセリンなど)を除いて、試験薬または同様の種類の作用の薬を受けません。 国際裁判では、通常、この期間が割り当てられます プラセボ.
対照期間および無作為化なしの試験(グループへのランダムな割り当て) は制御されているとは見なされないため、その結果には疑問があります。
各研究は明確に述べる必要があります 包含および除外基準研究からの患者。 それらがよく考えられているほど、結果の信頼性が高くなります。 例えば、抗虚血薬としてのβ遮断薬の有効性を研究する場合、硝酸塩やトリメタジジンなど、同様の効果を持つ他の薬を服用している患者を研究から除外する必要があります。
無作為化比較試験のデメリット
1) 選択したグループの非代表性、つまり 特定のサンプルが母集団全体の特性を正しく反映できないこと。 言い換えれば、このグループの患者について、この病理を持つすべての患者について真の結論を導き出すことは不可能です。
先ほど指摘したように、患者を研究に含めたり除外したりするための厳格な基準があります。 これは取得するために必要です 同質性比較できる患者のグループ。 通常、これらは最も深刻な患者ではありません。 重病の患者では、対照試験の厳格な要件を満たすことができません:対照期間、プラセボ、運動試験などの存在。
たとえば、研究では リタ(1993) 比較結果 経皮経管冠動脈形成術(管腔内のミニバルーンを膨らませることによる狭窄した動脈の拡張) 冠動脈バイパス移植(血液が動脈の狭窄部を通過するためのバイパスを作成します)。 研究が含まれていたので 患者のわずか3%冠動脈造影を受けた患者のうち、その結果を残りの 97% の患者に拡張することはできません。 サンプルは代表的なものではありません。
2) 利益相反.
いつ メーカーは多額の投資をしている彼の薬の臨床試験に参加する(つまり、実際に研究者の仕事にお金を払っている)ので、著者が肯定的な結果を得るためにあらゆる努力をしないとは信じがたい.
これらの理由から 単一の研究の結果は絶対に信頼できるとは言えません.
4
1 イヴァノヴォ州立大学
2 モスクワ物理工科大学 (国立大学) モスクワ州ドルゴプルドニ
3 ロシア連邦保健省の高等専門教育国家予算教育機関「Ivanovskaya GMA」
4 ロシア連邦保健省イヴァノヴォ州立医学アカデミー
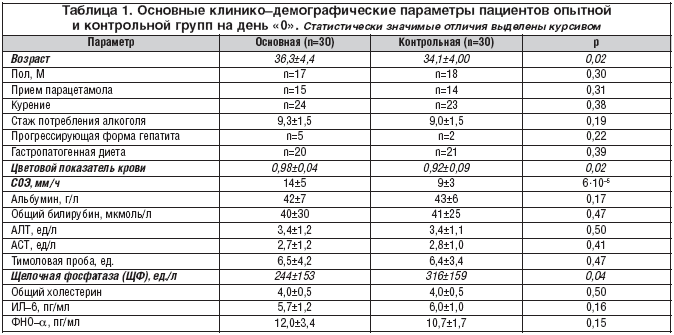
引用のために: Egorova E.Yu.、Yurgel I.S.、Nazarenko O.A.、Filosofova M.S.、Alper I.A.、Torshin I.Yu.、Yudina N.V.、Grishina T.R.、Gromova O.A. 慢性アルコール性肝炎 // BC 患者における Progepar の有効性のランダム化比較試験。 2011年第12号。 S. 753
はじめに 肝臓保護剤は、その薬理学的効果のメカニズムと範囲が異なります。 2008年、ロシアでは、肝保護剤(CodATC:A05BA)のグループで、薬剤Progeparが登録されました。 ドイツと日本では、この薬は「プロヘパルム S」として知られています。 以前に知られている薬「プロヘパー」とは、特別な相乗効果のある成分(薬の名前の文字「S」を意味します)の存在が異なります。







文学
1. Gromova O.A.、Torshin I.Yu.、Yurgel I.S. ら。 併用肝保護薬プロゲパーの作用機序と臨床効果。 困難な患者、2009 年、No. 12。
2. Bayashi A.O.、Akioma H.、Tatsaki H. 肝加水分解物の血液循環への影響 慢性疾患肝臓 //Artsnaimittel Forshung、- 1972、22C.578-580。
3. Fujisawa K.、Suzuki H.、Yamamoto S.、Hirayama C.、Shikata T.、Sanbe R. 慢性肝炎における肝加水分解物 Prohepar の治療効果 - 二重盲検対照試験。 アジア医学 J. 26(8):497-526
4. Demidov V.I.、Nazarenko O.A.、Egorova E.Yu. ら。 アルコールとパラセタモールによる実験的肝障害におけるプロゲパーの有効性の研究:生化学と組織学。 ファーマテカ、2011 年、第 2 号。
5. Egorova E.Yu.、Filosofova M.S.、Torshin I.Yu. ら。 Progeparによる治療中の持続型および進行型のアルコール性肝炎の比較動態。 ロシア医学ジャーナル、ロシア医学ジャーナル、第 19 巻、第 2 号、2011 年。
6. 2010 年 4 月 12 日の連邦法第 61-FZ 号「流通について」 薬» www.government.ru .
7. Ivashkin V.T.、Maevskaya M.V. 肝臓のアルコール性ウイルス性疾患。 - M.: Litterra, 2007. - 160 p.
8. Gromova O.A.、Satarina T.E.、Kalacheva A.G.、Limanova O.A. ビタミン欠乏症を評価するための構造化されたアンケート。 平成20年11月17日付合理化案第2461号
9. Zhuravlev Yu. I. Selected Scientific Works。 - M.: マスター、1998. - 420 p.
10. Zhuravlev Yu.I. 認識または分類の問題を解決するための代数的アプローチについて//サイバネティックスの問題:第33号..-1978.-p。 5-68。
11. Toguzov R.T.、Shachnev E.A.、Nazarenko O.A. ら。 肝保護剤プロゲパーの葉酸とリポ酸の含有量、Pharmateka、2011、3
12. Rebrov V.G.、Gromova O.A. ビタミン、マクロおよびマイクロエレメント。 GeotarMed, M., - 2008, 946 p.
13. Torshin I.Yu.、Gromova O.A. ビタミン D3 とがんの関係の生理学的モデルとエビデンスに基づく医療のデータ、難しい患者、2008 年、第 11 号、21 ~ 26 ページ
14. Isoda K, Kagaya N, Akamatsu S, Hayashi S, Tamesada M, Watanabe A, Kobayashi M, Tagawa Y, Kondoh M, Kawase M, Yagi K. ジメチルニトロソアミンによる肝障害に対するビタミン B12 の肝保護効果。 バイオ・ファーム・ブル。 2008 年 2 月;31(2):309-11。
